(广州市拓瑞科技有限公司 广东广州 510700)
摘要:以L-乳酸作为主要抑菌活性成分,对含L-乳酸的自制洗手液、湿巾样品进行抑菌性能测试。研究L-乳酸在洗手液、湿巾等清洁日用品中的抑菌效果。结果表明:在pH为4.2的洗手液中,1%的L-乳酸添加量,即可满足样品1:1稀释、2 min的测试条件下,对大肠杆菌、金黄色葡萄球菌的抑菌率均大于99.9%;在湿巾中,当pH值为4.1时,1%的L-乳酸即可满足2min测试条件下,湿巾样对大肠杆菌、金黄色葡萄球菌的抑菌率大于90%。
关键词:乳酸;抑菌;日用品;洗手液;湿巾;有机酸
新冠疫情的爆发和持续蔓延,强烈刺激了消费者的健康消费意识,对清洁日用品的需求不再仅仅满足于产品的基础功能。具有抑菌、除菌的日用品得到更多的消费者青睐。各类具有抑菌、抗菌的凝胶、洗手液、洗衣液、湿巾、除臭喷雾等日用品在各大电商平台争相上市。
在清洁日用消费品的市场上,产品类目及其繁多。而具有抑菌、抗菌性能的产品无外乎依赖于添加季铵盐类、胍类、酚类等具有消毒效果的成分,这些成分的产品在使用时具有潜在的皮肤刺激问题[1]。在清洁日用品更新迭代、开发时,开始出现温和、无刺激的抑菌活性成分,列如乳酸、抗菌肽、植物抑菌剂、银离子[2]等。
1 L-乳酸
1.1 L-乳酸的应用
乳酸是天然小分子有机弱酸,其分子骨架中羧基α位碳原子为不对称碳原子,可形成L(+)型和D(-)型两种旋光异构体。医学研究表明,人体具有L-乳酸脱氢酶而缺少D-乳酸脱氢酶,当D-乳酸进入人体后,过量的摄入会引起代谢紊乱等不良反应[3]。因此,在食品、饮料、医药、塑料、日用化工等领域使用的多为L-乳酸。
目前,L-乳酸的来源多为经淀粉、蔗糖、乳酸菌等发酵,再采用整合式一体化精制工艺提纯而来[4]。L-乳酸的应用非常广泛,在食品行业,常用于调味、保鲜、防腐等;在医药行业,常用于制剂、助溶、载体、消毒等;在日用品行业,常用于保湿、PH调节等。
1.2 L-乳酸的作用机理
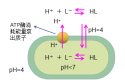
L-乳酸对革兰氏阳性菌和革兰氏阴性菌均有很强的抑制作用,其作用机理是多方面的,如图1,产品中L-乳酸的浓度和pH值对其抑菌效果影响十分明显[5]。
L-乳酸可透过微生物细胞膜,提高细胞内H+的浓度,当H+的供给超过能量供给,细胞能量失衡使细菌无法生存(a)。微生物细胞外高浓度的L-乳酸会阻断细胞内糖酵解产生乳酸的途径,从而抑制细菌生长(b)。L-乳酸分子进入细胞内,降低微生物细胞内的pH值,扰乱细胞膜的呼吸作用,造成细胞氧化应激,使细胞死亡(c)。


abc
图1 乳酸抑菌作用机理
人体皮肤表面的pH值范围为4.0~7.0,大部分为酸性,对于接触皮肤的产品呈酸性(pH<5)更有利于皮肤健康[6]。因此,在产品开发时偏酸性(pH<5.9)的产品更加符合皮肤健康理念,综合洗手液、凝胶、湿巾等清洁日用品的抑菌性能需求,L-乳酸无疑是一个很好的选择。
2 实验部分
2.1 主要试剂、材料和仪器
L-乳酸(HS90,活性物含量≥90%),Corbion;十二烷基苯磺酸(LAS,活性物含量90%±2%)、脂肪醇聚氧乙烯醚硫酸钠(AES-70,活性物含量≥70%),广州共信化工有限公司;烷基糖苷(APG2000,50%~53%),巴斯夫;椰油酰胺丙基甜菜碱(CAB-35,活性物含量35%)、椰子油脂肪酸二乙醇酰胺(6501,活性物含量85%),广州花之王化工有限公司;月桂酰肌氨酸钠(LS-30,活性物含量29%~31%),广州天赐;1,2-己二醇(活性物含量99.5%),Rickhan;苯甲酸钠(有效物含量99.8%),武汉有机;氢氧化钠(AR试剂)、二水合柠檬酸三钠(AR试剂)、磷酸氢二钾(AR试剂)、磷酸二氢钠(AR试剂),国药试剂。
营养琼脂培养基、孟加拉红营养琼脂培养基,广东环凯生物科技有限公司。
大肠杆菌Escherichia Coli ATCC 25922、金黄色葡萄球菌Staphylococcus Aureus ATCC 6538、白色念珠菌Candida Albicans ATCC 10231,广东省微生物菌种保藏中心。
洁净工作台,苏州净化设备有限公司;恒温培养箱BD260,德国宾得;恒温恒湿培养箱BPS-100CL,一恒科学仪器;数显加热板C-MAG HP 7,德国IKA;pH计FE28-Standard,梅特勒;电子天平BSA223S-CW,德国Sartoriu;1000ul移液枪、200ul移液枪,赛默飞。
2.2 实验方法
2.2.1 洗手液制样和抑菌性能测试
参考市场上常用的洗手液,根据表1的配方比例制作洗手液基料,先将配方80%去离子水和其他成分加入容器内,加热、搅拌使料体溶解、混匀,降温至40℃,再用NaOH溶液(10%)溶液调pH值至相应值,最后用去离子水补至配方100%,继续搅拌至均匀,得到稳定洗手液基料1、2、3、4。
表1 洗手液基料配比
成分 | 洗手液2 | 洗手液3 | 洗手液4 |
80% 去离子水 | 80% 去离子水 | 80% 去离子水 | 80% 去离子水 |
2% LAS | 2% LAS | 2% LAS | 6% AES70 |
6% AES70 | 6% AES70 | 6% AES70 | 4% APG2000 |
2% APG2000 | 2% APG2000 | 2% APG2000 | 4% CAB35 |
2% 6501 | 2% 6501 | 2% 6501 | 1.0% HS90 |
1.0 % HS90 | 1.0 % HS90 | ||
NaOH溶液调pH至4.2 | NaOH溶液调pH至4.2 | NaOH溶液调pH至4.6 | NaOH溶液调pH至4.2 |
去离子水补至100% | 去离子水补至100% | 去离子水补至100% | 去离子水补至100% |
参照GB/T 15979-2002 一次性卫生用品卫生标准-附录C4,取稀释(1:1)后的样品洗手液1、2、3、4和磷酸盐缓冲体系(PBS)对照组各5.00ml,分别加入预先准备好的菌悬液100ul(大肠杆菌Escherichia Coli ATCC 25922、金黄色葡萄球菌Staphylococcus Aureus ATCC 6538),计时并快速混匀,作用2min后,吸取反应液用PBS做10倍梯度稀释,吸取1ml每个梯度的稀释液置于2个平皿内,倾注预冷(45℃~50℃)的营养琼脂培养基或孟加拉红营养琼脂培养基,待琼脂冷却凝固,将平板置于恒温培养箱(细菌,37℃,48h),做菌落计数,记录实验结果,计算样品洗手液的抑菌率。结果如表2。
表2 洗手液的抑菌效果
样品编号 | 微生物种类 | 回收菌落数/(cfu/ml) | 抑菌率/% |
PBS对照 | 大肠杆菌 | 7.3×104 | / |
金黄色葡萄球菌 | 8.9×104 | / | |
洗手液1 | 大肠杆菌 | 6.1×104 | 16.4 |
金黄色葡萄球菌 | 8.7×104 | 2.2 | |
洗手液2 | 大肠杆菌 | <10 | >99.9 |
金黄色葡萄球菌 | <10 | >99.9 | |
洗手液3 | 大肠杆菌 | 7.8×102 | 98.9 |
金黄色葡萄球菌 | 1.3×103 | 98.5 | |
洗手液4 | 大肠杆菌 | 5.8×102 | 99.2 |
金黄色葡萄球菌 | <10 | >99.9 |
2.2.2 湿巾制样和抑菌性能测试
根据表3的配方比例制备湿巾液,在容器内加入90%的无菌去离子水,其他成分依次加入,加热搅拌至完全溶解,降温至40℃,用10%含量的柠檬酸三钠调pH至相应值,再以无菌去离子水补至配方100%,继续搅拌至均匀,得到均匀、稳定的湿巾液。以全棉水刺无纺布作为基础布,按照1:4的质量比,将全棉水刺无纺布沉浸在湿巾液中,制得湿巾样品。
表3 湿巾液的成分比例
成分名称 | 湿巾液1 | 湿巾液2 |
去离子水 | 98.5% | 98.5% |
1,2-己二醇 | 0.3% | 0.3% |
月桂酰肌氨酸钠 | 0.1% | 0.1% |
苯甲酸钠 | 0.1% | 0.1% |
HS90 | 1.0% | 1.0% |
柠檬酸三钠(10%) | 调pH至4.1 | 调pH至4.5 |
参照WS/T650-2019 抗菌和抑菌效果评价方法5.13-载体抑菌实验,将湿巾样和润湿的全棉水刺无纺布裁剪成0.20 cm *0.30 cm的样片,在样片上均匀滴加预先准备好的菌悬液100ul(大肠杆菌Escherichia Coli ATCC 25922、金黄色葡萄球菌Staphylococcus Aureus ATCC 6538、白色念珠菌Candida Albicans ATCC 10231),计时,作用2min后,将样片转至5.00ml的PBS中,混匀、振荡洗脱,吸取洗脱液用PBS做10倍梯度稀释,吸取1ml每个梯度的稀释液置于2个平皿内,倾注预冷(45℃~50℃)的营养琼脂培养基或孟加拉红营养琼脂培养基,待琼脂冷却凝固,将平板置于恒温培养箱(细菌,37℃,48h)或恒温恒湿培养箱(酵母菌,30℃,72h),做菌落计数,记录实验结果,对比全棉水刺无纺布样计算湿巾样的抑菌率。结果如下表4。
表4 湿巾的抑菌效果
样品标号 | 微生物种类 | 回收菌落数/(cfu/片) | 抑菌率/% |
空白对照组 | 大肠杆菌 | 2.8×104 | / |
金黄色葡萄球菌 | 7.6×104 | / | |
白色念珠菌 | 2.6×104 | / | |
湿巾1 | 大肠杆菌 | 95 | 99.7% |
金黄色葡萄球菌 | 1.7×102 | 99.8% | |
白色念珠菌 | 2.2×104 | 15.4% | |
湿巾2 | 大肠杆菌 | 4.3×103 | 84.6% |
金黄色葡萄球菌 | 7.2×103 | 90.5% | |
白色念珠菌 | 2.3×104 | 11.5% |
3 结果与讨论
3.1 洗手液抑菌测试结果
如上表2,1.0%的L-乳酸(HS90)添加量,在1:1稀释、2min接触时间的测试条件下,洗手液1对测试菌基本没有抑菌效果,而洗手液2、3、4都有很高的抑菌率,可见洗手液的抑菌效果主要来源于L-乳酸(HS90)。洗手液1对大肠杆菌、金黄色葡萄球菌抑菌率均大于99.9%;洗手液3对大肠杆菌、金黄色葡萄球菌抑菌率分别为98.9%、98.5%;可见洗手液的pH值为4.2时的抑菌率明显高于pH为4.6时的洗手液,pH值对洗手液的抑菌率影响明显,pH值越低抑菌率越高。洗手液4对大肠杆菌、金黄色葡萄球菌抑菌率分别为99.2%、大于99.9%;可见除pH值外,洗手液的表面活性剂成分也会影响其抑菌率。
2.4.2 湿巾抑菌测试结果
如上表4,1.0%添加量的L-乳酸(HS90)湿巾液制成的湿巾,在2min的接触时间条件下,湿巾1(pH=4.1)对大肠杆菌的抑菌率为99.7%,对金黄色葡萄球菌的抑菌率为99.8%,对白色念珠菌的抑菌率为15.4%;湿巾2(pH=4.5)对大肠杆菌的抑菌率为84.6%,对金黄色葡萄球菌的抑菌率为90.5%,对白色念珠菌的抑菌率为11.5%。可见含L-乳酸的湿巾对大肠杆菌和金黄色葡萄球菌具有很高的抑菌率,且随着湿巾液的pH升高,对大肠杆菌和金黄色葡萄球菌的抑菌率明显下降。但上表4显示,湿巾对白色念珠菌的抑菌率分别为15.4%、11.5%,没有表现出抑菌效果。
3 总结
L-乳酸作为即时抑菌活性物应用时,有很明显的抗微生物活性,但在实际应用时仍有一定短板。L-乳酸的抑菌活性主要依赖于L-乳酸分子和H+的浓度,所以在实际应用时,L-乳酸的添加量太低或者pH太高都难以发挥L-乳酸应有的抑菌能力;并且L-乳酸具有明显的抗菌选择性,L-乳酸可以表现出对革兰氏阳性、革兰氏阴性菌良好的抑制能力,但是对细胞壁、细胞膜更厚的真菌则难有抑制作用。
在产品开发、应用时,特别是洗涤清洁产品,其低pH的抑菌条件要求可能会使产品遇到洗涤能力降低、难增稠、稳定性等问题。但是,L-乳酸良好的抑菌性能,综合其温和、保湿等性能特效,决定L-乳酸是很好的日用品抑菌基础原材料,在洗手液、沐浴露、洗衣液、洗洁精、湿巾、除味喷剂等产品领域必将迎来更广阔的的应用前景。
参考文献:
[1]曲召辉,吕永博,刘有停等.消毒杀菌类产品的皮肤刺激性及护理研究[J].中国洗涤用品工业,2020(Z1):75-79.
[2]雷敏,于文.市售洗手液用抑菌剂的介绍及其发展[J].中国洗涤用品工业,2021(08):26-31.
[3]Expert Committee on food Additives.Lactic acid[R].WHO Food Add,1967,29;144-148.
[4]汪多仁.L-乳酸的开发与应用进展[J].粮食加工,2009(01):44-47.
[5]汪陈洁.乳酸对常见食源性致病菌的抗菌活性与作用机理[D].湖北:华中农业大学2015.
[6]姜姗姗,李燕,韩婷婷等.皮肤酸性pH值与化妆品研发[J].日用化学品科学,2022(05):48-51.