(1.汕头大学医学院,广东省汕头市,邮编515041;2.汕尾市第二人民医院,广东省汕尾市,邮编516600;3.汕头大学医学院第一附属医院,广东省汕头市,邮编515041)
摘要:【目的】:探讨恩杂鲁胺联合雄激素剥夺治疗对于转移性去势抵抗性前列腺癌患者的疗效、生活质量以及安全性。【方法】分析2019年7月至2022年6月期间汕大附一院采用阿比特龙及恩杂鲁胺治疗的患者资料。采用对照研究分组。入组标准:未接收化疗,使用比卡鲁胺、阿帕他胺等抗雄治疗后PSA倍增时间为3个月或更少的持续性雄激素剥夺的转移性去势抵抗性前列腺癌患者。治疗组接受口服恩扎鲁胺(160毫克/天),对照组口服阿比特龙(1000mg/天)。观察指标:接受治疗至无进展生存期(定义为从治疗开始到影像学进展的时间或到无影像学进展的死亡时间)的时间、接受治疗后PSA应答率、PSA发生进展时间、前列腺癌患者生存质量FACT-P评分下降时间,以及治疗过程中发生的不良反应。
【结果】共69例患者入组接受了治疗。其中恩杂鲁胺治疗组39例,阿比特龙对照组30例。截至2023年3月 31日,恩扎鲁胺组的中位无影像学进展生存时间为16.6个月 ,而对照组的中位无影像学进展生存时间为13.2个月。恩扎鲁胺组PSA应答率为92.3%,对照组的PSA应答率为83.3%(P=0.281)。恩扎鲁胺组中位无PSA进展时间为12.6个月,对照组为9.75个月(P=0.017)。恩扎鲁胺组中位FACT-P评分无下降时间为17个月,对照组为12个月(P=0.012)接受恩扎鲁胺治疗的患者中,33.3%发生3级或以上的不良事件,而接受阿比特龙治疗的患者中这一比例为43.3%(P=0.395)。【结论】恩杂鲁胺治疗转移性去势抵抗性前列腺癌,能有效延缓转移及PSA的进展,改善患者生活质量,安全性良好。
关键词:去势抵抗性前列腺癌;恩杂鲁胺;阿比特龙;疗效
1.研究背景
前列腺癌是最常见的男性泌尿生殖系统恶性肿瘤之一。2021年2月 WHO 国际癌症研究机构发表的全球癌症统计报告(2020年版)显示全球新发前列腺癌发病率仅次于乳腺癌和肺癌,位于第 3 位,死亡率位居第 8 位。在亚洲及我国,前列腺恶性肿瘤的发病率和死亡率都在迅速升高[1]。因此,前列腺癌的精准诊疗是目前全球医疗界亟需解决的临床问题。雄激素受体(Androgen Receptor, AR)是前列腺癌的发生和发展关键影响因子。转录因子AR受雄激素激活调控,雄激素与AR的结合可启动AR调控的基因表达,从而驱动前列腺癌细胞的生长。前列腺癌的重要治疗手段之一是雄激素剥夺疗法(Androgen Deprivation Therapy,ADT),其目的是抑制雄激素的产生或阻断其激活AR的途径,主要方式有手术去势及药物去势[2]。国内常见的治疗药物有比卡鲁胺、氟他胺以及近些年扩大治疗范围的新型抗雄药物阿比特龙。近年来,已有多种新型内分泌药物如阿比特龙、恩杂鲁胺、阿帕他胺等用于前列腺癌的治疗中,并取得一定的临床疗效[3]。有研究表明,阿比特龙联合 ADT 能明显延长转移性激素敏感性前列腺癌(metastatic hormone- sensitive prostate cancer,mHSPC)和转移性去势抵抗性前列腺癌(metastatic castration- resistant prostate cancer, mCRPC)患者的总生存期(overall survival,OS)及影像学无进展生存期(ray progression-free survival,rPFS)[4] 。但随之而来的是该类药物的治疗都不可避免地产生去势抵抗。恩扎鲁胺是一种新型的雄激素受体通道的抑制剂,在国外的报道中可以延长转移性、去势耐药前列腺癌患者的总生存期。为此我们设计的研究方案为通过检测影像学转移病灶的改变及PSA水平,研究恩杂鲁胺在治疗转移性去势抵抗性前列腺癌患者中的临床疗效。
2.研究方法
2.1研究设计
我们进行了回顾性病例对照研究,收集汕头大学医学院第一附属医院泌尿外科2019年7月至2022年6月收治的mCRPC患者69例。其中恩扎鲁胺治疗组纳入39名患者,治疗方案为口服恩杂鲁胺(160毫克/天)加雄激素剥夺治疗,另外阿比特龙治疗组纳入30名患者,治疗方案为口服醋酸阿比特龙(1000mg/天)联合服用泼尼松加雄激素剥夺治疗。
2.2研究对象
所有符合入组条件的患者均行前列腺穿刺检查,病理确诊为前列腺癌,且不伴有神经内分泌分化、印戒细胞特征或小细胞特征。所有患者必须接受过促性腺激素释放激素激动剂或拮抗剂的雄激素剥夺治疗,或接受双侧睾丸切除术。患者还必须有至少三次PS
A出现上升,间隔至少1周,基线PSA水平2ng/ml或更大,PSA倍增时间3个月或更少,通过磁共振检查评估软组织病灶和全身放射性核素骨扫描以确定转移病灶的范围和大小。排除患有疑似脑转移或活动性软脑膜疾病,或有癫痫发作史或可能导致癫痫发作易感性的患者。研究时间截止到出现影像学进展的时间或2023年3月31日,并再次通过影像学检查进行评估。
2.3观察指标
2.3.1主要终点 主要终点为无进展生存期,定义为从分组到影像学进展的时间。影像学进展定义:治疗期间随访过程中出现影像学新发转移病灶或所有原转移病灶短径总和增加至少20%[5]。
2.3.2次要终点 次要终点包括PSA进展的时间、PSA反应率(以≥较基线下降50%为完全应答;较基线下降<50%的为部分应答;PSA升高的为无应答)。
2.3.3不良反应发生率统计治疗结束后患者的不良事件发生率。
2.3.4其他指标比如前列腺癌患者生活质量FACT-P评分下降。每4周复测一次血PSA、碱性磷酸酶、睾酮、血红蛋白等生化指标。每3个月进行一次影像学检查,直到影像学进展。由放射科医生及临床医生根据实体肿瘤反应评估确定疾病进展的状态。
2.4统计分析
采用软件 SPSS 26.0处理汇总的所有数据,并加以分析。服从正态性的计量资料用均数±标准差表示,用t检验比较;不服从正态分布的计量数据用中位数(四分位数间距)表示,用Mann-Whitney u 检验比较。计数资料用卡方检验,无进展生存率、PSA无进展时间、FACT-P评分无下降时间利用 Kaplan-Meier 生存分析绘制生成生存曲线图,利用 Log-rank 检验法进行差异性比较两组无进展生存率,P<0.05代表检验结果具有统计学差异。
3研究结果
3.1一般情况
2019年7月至2022年6月,共统计了69例患者资料。接受治疗前均有前列腺穿刺病理结果确诊为前列腺癌患者,MR证实已转移或多处转移。经抗雄去势内分泌治疗产生抵抗。研究对象中接受恩扎鲁胺治疗组39例,30人接受阿比特龙治疗为对照组。患者的一般资料见表1。
表1.患者的一般资料
特征 | 恩扎鲁胺(n=39) | 阿比特龙(n=30) | P值 |
年龄(岁) | 70(60-77) | 67(62-72) | 0.389 |
BMI(kg/m2) | 21.53±3.53 | 22.01±3.36 | 0.572 |
ECOG评分 | 0.012 | ||
0 | 16(41.0) | 5(16.7) | |
1 | 16(41.0) | 23(76.7) | |
2 | 7(17.9) | 2(6.7) | |
T分期 | 0.187 | ||
T2 | 7(17.9) | 2(6.7) | |
T3 | 22(56.4) | 23(76.7) | |
T4 | 10(25.6) | 5(16.7) | |
淋巴结转移 | 0.197 | ||
有 | 16(41) | 17(56.7) | |
无 | 23(59) | 13(51.5) | |
内脏转移 | 0.616 | ||
有 | 33(84.6) | 24(80) | |
无 | 6(15.4) | 6(20) | |
骨转移灶 | 0.562 | ||
≤6 | 22(56.4) | 19(63.3) | |
>6 | 17(43.6) | 11(36.7) | |
用药前PSA(ng/ml) | 14.21±5.42 | 11.85±4.94 | 0.068 |
3.2结果
3.2.1主要研究终点
在截止至2023年3月31日,恩扎鲁胺组28例患者(71.8%)和阿比特龙组26例患者(86.7%)发生了主要终点事件,即发生影像学进展。恩扎鲁胺组中位随访时间为21(18-26)个月,阿比特龙组中位随访时间为18.5(15-23.5)个月。恩扎鲁胺组中位影像学无进展生存期为12.6个月,而阿比特龙组为13.2个月。mCRPC患者出现影像学进展的时间和两种药物疗效的关系通过Kaplan-Meier生存分析生成生存曲线来展示,两组的PFS无明显统计学差异(Log-rank P=0.169)见图1。

图1.恩杂鲁胺组与阿比特龙组的PFS的 Kaplan-Meier 生存分析曲线
3.2.2次要研究终点
随访期间,在恩扎鲁胺组,38例(97.4%)患者在服用恩扎鲁胺后出现PSA应答:其中36例(92.3%)患者为PSA完全应答,平均应答时间为用药后2个月;2例患者表现为PSA部分应答,比率为5.1%。还有1例(2.6%)患者表现为PSA无应答。随访期间28例患者出现PSA进展,中位PSA无进展时间为12.6(7.2-18.6)个月。对照组服用阿比特龙后随访发现,PSA完全应答的有25例(83.3%),部分应答的有3例(10%),还有2例(6.7%)表现为PSA无应答。随访期间26例患者出现PSA进展,中位PSA无进展时间为9.75(4.3-14.3)个月。两组在PSA反应率及进展率上无明显差异(P>0.05),但在PSA最低值(P=0.041)及中位PSA无进展时间(Log-rank P=0.017)上恩扎鲁胺表现更加优秀(表2)。 mCRPC 患者出现PSA进展的时间和两种药物疗效的关系通过 Kaplan-Meier 生存曲线图展示(图2)。
表2.两组患者的PSA进展情况对比
观察指标 | 恩扎鲁胺(n=39) | 阿比特龙(n=30) | P值 |
PSA反应率(%) | 97.4(38) | 93.3(28) | 0.505 |
PSA最低值(ng/ml) | 0.19(0.09-0.82) | 0.73(0.12-2.32) | 0.041 |
PSA进展率(%) | 73.7(28) | 86.7(26) | 0.242 |
中位PSA无进展时间(m) | 12.6(7.2-18.6) | 9.75(4.3-14.3) |
图2.恩杂鲁胺组与阿比特龙组的PSA进展时间的 Kaplan-Meier 生存分析曲线
![]() 3.2.3药物安全性
3.2.3药物安全性
两种药物治疗出现不良事件见表3。出现3级或更高级别的不良事件的比例两组无明显差异(P=0.395)。因不良事件而停止试验的恩扎鲁胺组有1例。因不良事件而停止试验的阿比特龙组有1例。在恩杂鲁胺组患者中最常见的不良事件为疲劳,其中4例为3级不良事件,出现潮热、血糖升高、眩晕的3级不良事件为6例。对照组阿比特龙治疗后常见并发症为肝功能损害、消化道不良反应及低血钾。
表3.恩扎鲁胺的3级及以上不良反应
不良反应 | 恩扎鲁胺(n=39) | 阿比特龙(n=30) |
乏力 | 4 | 0 |
潮热 | 2 | 0 |
消化道症状 | 1 | 3 |
疼痛 | 1 | 1 |
转氨酶升高 | 0 | 2 |
低血钾 | 0 | 3 |
高血压 | 1 | 1 |
血糖升高 | 2 | 2 |
眩晕 | 2 | 0 |
泌尿系感染 | 0 | 1 |
比例(%) | 33.3(13) | 13(43.3) |
3.2.4患者生存质量评估
我们采用癌症治疗-前列腺功能评估(FACT-P)量表对前列腺癌患者的生活质量进行评分,得分范围为0至156,得分越高,表明健康相关的生活质量越好。FACT-P评分的下降定义为每个患者的总体评分比基线评分下降至少10分。随访期间,在恩扎鲁胺组,24例(61.5%)的患者在服用恩扎鲁胺后出现FACT-P下降,中位FACT-P下降时间为17(12-20)个月。对照组服用阿比特龙后随访发现,26例(86.7%)的患者在服用恩扎鲁胺后出现FACT-P下降,中位FACT-P下降时间为12(7-20)个月。两组无论是在FACT-P下降率(P=0.029)还是中位FACT-P下降时间(Log-rank P=0.012)上均有统计学差异。mCRPC 患者出现FACT-P下降的时间和两种药物的关系通过Kaplan-Meier 生存曲线图来展示(图3)。
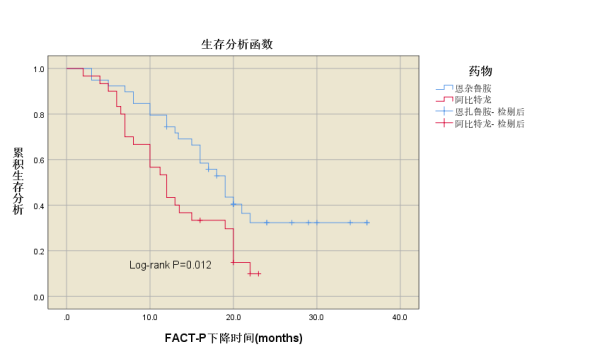
图3.恩杂鲁胺组与阿比特龙组的FACT-P下降时间的 Kaplan-Meier 生存分析曲线
4.讨论
恩扎鲁胺可以直接与雄激素受体结合,起到抑制雄激素结合、雄激素受体核易位和雄激素受体介导的DNA结合的作用[6]。它对总生存期的影响已在两项国际3期试验中有报道,涉及转移性去势耐药前列腺癌患者[7-8]。国内有学者认为在恩扎鲁胺对阿比特龙耐药后的CRPC患者进行替换治疗,可有效延缓部分患者肿瘤进展[5]。此外,在一项随机、对照的比卡鲁胺II期临床试验中,对于既往未接受过化疗的患者,恩扎鲁胺治疗延长了非转移性前列腺癌患者的影像学无进展生存期。在非转移性去势抵抗性前列腺癌且PSA值迅速上升的男性中,恩扎鲁胺治疗的无转移生存时间、PSA无进展时间以及随后首次使用抗肿瘤治疗的时间均明显长于阿比特龙组(P<0.001) 。恩扎鲁胺治疗组出现转移或死亡的风险比安慰剂组低71%[9]。在所有亚组中,都观察到恩扎鲁胺治疗对无进展生存期的延长。在本项研究中,虽然恩扎鲁胺治疗组与阿比特龙组在PFS和PSA反应率上无明显统计学差异,但是在PSA最低值和PSA无进展时间上恩扎鲁胺的表现优于阿比特龙。一项关于恩扎鲁胺对非转移性去势抵抗性前列腺癌的临床研究结果显示,恩扎鲁胺组治疗非转移性去势抵抗性前列腺癌症患者的无转移中位生存期比安慰剂组延长10个月以上,即使该项研究的基线数据只评估了骨转移,对基线PSA加倍时间没有进行限制。PSA在前列腺癌治疗中具有重要的指向作用。国内有学者认为PSA进展与影像学进展分离的现象较为常见,部分影像学进展初期的患者PSA尚未出现进展[5]。恩扎鲁胺的安全性与之前针对去势抵抗性前列腺癌症患者的临床试验报告一致。[10-11]。本研究中恩扎鲁胺组患者发生3级或以上不良事件的比率略低于阿比特龙组。恩扎鲁胺组的乏力及潮热事件报告频率高于阿比特龙组,而接受阿比特龙治疗的患者比接受恩扎鲁胺治疗的患者更常见电解质异常和肝功能损害。当然我们还需要更大样本进行进一步的安全性分析,以评估不同的患者亚组是否有更高的风险发生这些不良事件。众所周知,CRPC的治疗的目标主要是为了延缓转移的疾病进展,以减轻癌症相关症状,并延长总生存期,另一方面,患者生存质量对于药物的选择也具有重大意义[12-13]。在本项研究中,我们采用癌症治疗-前列腺功能评估(FACT-P)量表对前列腺癌患者的生活质量进行评分,结果发现服用恩扎鲁胺的患者在生存质量方面相对阿比特龙来说更加有保障,可以显著延长患者生存质量发生下降的时间。
总之,我们的研究表明恩杂鲁胺治疗去势抵抗性前列腺癌,能有效延缓PSA的进展
。两者的安全性没有明显差异。在生活质量上,恩扎鲁胺对患者的保护优于阿比特龙。
作者简介:李四化,泌尿外科主任医师,研究领域:泌尿外科疾病的微创治疗及泌尿肿瘤的综合治疗,E-mail:2804517@qq.com;林明恩,通信作者,教授,硕士生导师,E-mail:me_lin20@163.com
参考文献:
[1]2022年版前列腺癌诊疗指南.
[2]蔡汶洁. LRRN1促进去势抵抗性前列腺癌恩杂鲁胺耐药的作用及机制研究[D].山东大学,2021.DOI:10.27272/d.cnki.gshdu.2021.005603.
[3]Tafuri A, Cerruto MA, Antonelli A. Neoadjuvant strategies before radical prostatectomy for high risk prostate cancer in the era of new hormonal agents[J]. Curr Drug Targets,2021, 22(1): 68-76.
[4]曾瑞琪,袁开盛,兰瑾涛等.新型内分泌药物在前列腺癌新辅助治疗中的应用[J].癌症进展,2022,20(06):559-560+588.
[5]张峰波,朱熹,吉正国等.恩扎卢胺治疗阿比特龙耐药的转移性去势抵抗性前列腺癌19例疗效观察[J].现代泌尿外科杂志,2021,26(07):574-577.
[6]Tran C, Ouk S, Clegg NJ, et al. Development of a second-generation antiandrogen for treatment of advanced prostate cancer. Science 2009;324:787-90.
[7]Beer TM, Armstrong AJ, Rathkopf DE, et al. Enzalutamide in metastatic prostate cancer before chemotherapy. N Engl J Med 2014;371:424-33.
[8]Scher HI, Fizazi K, Saad F, et al. Increased survival with enzalutamide in prostate cancer after chemotherapy. N Engl J Med 2012;367:1187-97.
[9]Hussain M, Fizazi K, Saad F, Rathenborg P, Shore N, Ferreira U, Ivashchenko P, Demirhan E, Modelska K, Phung D, Krivoshik A, Sternberg CN. Enzalutamide in Men with Nonmetastatic, Castration-Resistant Prostate Cancer. N Engl J Med. 2018 Jun 28;378(26):2465-2474.
[10]Smith MR, Kabbinavar F, Saad F, et al. Natural history of rising serum prostate specific antigen in men with castrate nonmetastatic prostate cancer. J Clin Oncol 2005;23:2918-25.
[11]Smith MR, Cook R, Lee KA, Nelson JB. Disease and host characteristics as predictors of time to first bone metastasis and death in men with progressive castration-resistant nonmetastatic prostate cancer. Cancer 2011;117:2077-85.
[12]Nelson JB, Love W, Chin JL, et al. Phase 3, randomized, controlled trial of atrasentan in patients with nonmetastatic, hormone-refractory prostate cancer. Cancer 2008;113:2478-87.
[13]Miller K, Moul JW, Gleave M, et al. Phase III, randomized, placebo-controlled study of once-daily oral zibotentan (ZD4054) in patients with non-metastatic castration-resistant prostate cancer. Pros
tate Cancer Prostatic Dis 2013;16:187-92.