凉山州民族中学
一、问题提出
人民教育出版社全日制普通高级中学教科书(必修加选修)《化学》第二册第16页演示实验1-7演示了铜与浓硝酸反应的实验。这个实验能达到一定的教学效果。但从绿色、环保的角度考虑还存在下列问题。
1、在反应发生后再塞上塞子,此时已有少量的NO2气体逸到空气中,这对环境造成污染,也不利于教师的身体健康;
2、书本上的实验装置不能控制反应的随时进行,达不到随用随反应的实验要求。
3、书本上的实验装置须把其中的一种药品(铜片或浓HNO3)反应完全后,反应才能终止。
4、书本上实验装置的吸收装置容易发生倒吸现象。
二、实验的设计思路
1、采用封闭实验体系进行反应,减少有害气体的排放;
2、反应前铜片与浓HNO3先分离,在需要产生NO2气体时才使两种药品接触,不需要NO2气体时使两种反应物分离,从而使反应终止。
三、实验原理
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
2NO2+2NaOH=NaNO2+NaNO3+H2O
四、改进后的实验装置
![]()
![]()
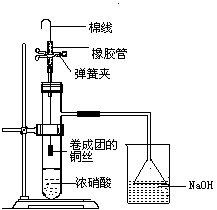 图(1)
图(1)  图(2)
图(2)
五、操作步骤
1、按图(1)、图(2)组装好实验仪器,检查装置气密性;
2、将浓HNO3注入试管(或具支试管),并塞上塞子;
3、将导气管的另一端通入盛有NaOH溶液的烧杯中;
4、打开弹簧夹,把铜丝放入到浓HNO3中;
5、反应结束后,打开弹簧夹,把铜丝提出液面使反应停止,并夹紧弹簧夹。
六、实验现象
可以看到铜丝表面有大量的气泡产生,溶液颜色逐渐变为蓝绿色,在液面上有大量的红棕色气体生成,并逐渐上升,从导气管导出被NaOH溶液吸收。
七、实验优点
1、采用该装置进行实验,能有效防止NO2对空气的污染,保护教师的身体健康,有助于增强学生的环保意识;
2、气处理装置能有效防止溶液的倒吸;
3、实验现象明显,增强直观效果,操作简便,成功率高;
4、该装置有启普发生器的优点,对于气体能随用随取,可以作NO2的制取装置;
5、节约药品。